Em uma das etapas de tratamento da água, ocorre a…
(CEFET-PR) Em uma das etapas de tratamento da água, ocorre a retenção de partículas sólidas em uma massa gelatinosa constituída de hidróxido de alumínio. Essa substância é preparada pela adição de Ca(OH)2 e Aℓ2(SO4)3 à água contida em tanques de tratamento. O número de mols de Aℓ2(SO4)3 que devem reagir com suficiente Ca(OH)2 para formar 10 mol de hidróxido de alumínio é igual a:
a) 1
b) 2
c) 3
d) 4
e) 5
Resolução
Equação química balanceada do processo de formação do hidróxido de alumínio:
3 Ca(OH)2(aq) + Aℓ2(SO4)3(aq) → 2 Aℓ(OH)3 + 3 CaSO4(aq)
De acordo com a equação acima, a proporção estequiométrica é de 2 mols de Aℓ(OH)3 formados para cada mol de Aℓ2(SO4)3 que reage. Logo, a quantidade em mols de Aℓ2(SO4)3 necessária para produzir 10 mols de Aℓ(OH)3 é dada por:
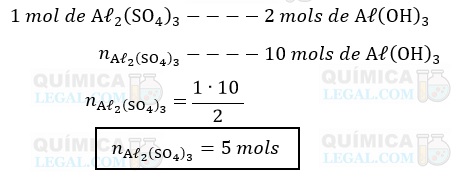
Portanto, são necessários 5 mols de sulfato de alumínio para produzir 10 mols de hidróxido de alumínio.
Gabarito: LETRA E
Confira mais EXERCÍCIOS RESOLVIDOS sobre ESTEQUIOMETRIA.
Tá afim de ver mais RESOLUÇÕES COMENTADAS do CEFET?

