(Enem 2009) Para que apresente condutividade elétrica adequada a muitas aplicações, o cobre bruto obtido por métodos térmicos é purificado eletroliticamente. Nesse processo, o cobre bruto impuro constitui o ânodo da célula, que está imerso em uma solução de CuSO4. À medida que o cobre impuro é oxidado no ânodo, íons Cu2+ da solução são depositados na forma pura no cátodo. Quanto às impurezas metálicas, algumas são oxidadas, passando à solução, enquanto outras simplesmente se desprendem do ânodo e se sedimentam abaixo dele. As impurezas sedimentadas são posteriormente processadas, e sua comercialização gera receita que ajuda a cobrir os custos do processo. A série eletroquímica a seguir lista o cobre e alguns metais presentes como impurezas no cobre bruto de acordo com suas forças redutoras relativas.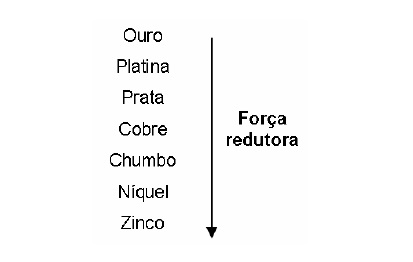
a) Au, Pt, Ag, Zn, Ni e Pb.
b) Au, Pt e Ag.
c) Zn, Ni e Pb.
d) Au e Zn.
e) Ag e Pb.
Resolução
Força redutora em eletroquímica pode ser basicamente definida como: a capacidade de um metal sofrer oxidação e consequentemente provocar a redução de outro elemento.
De acordo com a série eletroquímica apresentada no enunciado, podemos separar os metais em dois grupos:
- Força redutora maior do que a do cobre (Cu): Zinco (Zn), níquel (Ni) e chumbo (Pb).
- Força redutora menor do que a do cobre (Cu): Prata (Ag), Platina (Pt) e Ouro (Au).
Ainda segundo o enunciado, o cobre impuro é oxidado no ânodo e os íons Cu2+ são depositados (reduzido) na forma pura no cátodo.
As impurezas metálicas com força redutora maior que a do cobre (Zn, Ni e Pb) serão oxidados e ficarão na forma de íons na solução. Por outro lado, as impurezas metálicas com força redutora menor do que o cobre (Au, Ag e Pt) não são oxidadas e vão se desprender do ânodo e formarão a lama anódica, ou seja, vão sedimentar abaixo do ânodo.
Portanto, a alternativa correta é a letra B.
Gabarito: LETRA B
Confira mais EXERCÍCIOS RESOLVIDOS sobre ELETROQUÍMICA.
Tá afim de ver mais RESOLUÇÕES COMENTADAS do ENEM?

