O ácido fosfórico, usado em refrigerantes do tipo…
(UFSM-RS) O ácido fosfórico, usado em refrigerantes do tipo “cola” e possível causador da osteoporose, pode ser formado a partir da equação não balanceada:
Ca3(PO4)2 + H2SO4 → H3PO4 + CaSO4
Partindo-se de 62 g de Ca3(PO4)2 e usando-se quantidade suficiente de H2SO4, qual será, em gramas, a massa aproximada de H3PO4 obtida?
a) 19
b) 25
c) 39
d) 45
e) 51
Resolução
Equação química balanceada:
Ca3(PO4)2 + 3 H2SO4 → 2 H3PO4 + 3 CaSO4
De acorco com a equação química balanceada, são produzidos 2 mols de H3PO4 para cada mol de Ca3(PO4)2 que reage. Assim, temos:
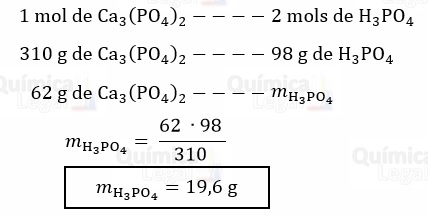
Gabarito: LETRA A
Confira mais EXERCÍCIOS RESOLVIDOS de ESTEQUIOMETRIA.
Tá afim de ver mais RESOLUÇÕES COMENTADAS da UFSM?



