Os quatro cilindros de um novo tipo de motor de combustão têm…
(Princípios de Química, Atkins) Os quatro cilindros de um novo tipo de motor de combustão têm, cada um, um deslocamento de 3,60 L. (Em outras palavras, o volume de cada cilindro se expande 3,60 L cada vez que o combustível entra em ignição.)
a) Se cada pistão dos quatro cilindros é movido com uma pressão de 1,80 Kbar e ocorre ignição nos cilindros a cada segundo, quanto trabalho o motor é capaz de executar em 1,00 minutos?
b) O trabalho é positivo ou negativo em relação ao motor e seus componentes?
Resolução
O trabalho de expansão (W), que é o tipo de trabalho provocado por uma mudança no volume de um sistema, é dado pela seguinte fórmula:
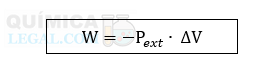
Onde
- W = trabalho
- Pext = pressão externa
- ΔV = variação do volume (Vfinal – Vinicial)
De acordo com o enunciado, os cilindros são movidos com uma pressão 1,80 kbar, ou seja, Pext = 1.800 bar. E a variação do volume é igual ao deslocamento do cilindro, ou seja, ΔV = 3,60 L. A unidade de trabalho é o joule (J).
Entendendo que 1 Joule (J) é equivalente a Pascal (Pa) multiplicado por metro cúbico (m3), é necessário realizar a conversão da pressão de kilobar (kbar) para Pascal (Pa) e do volume de litros (L) para metros cúbicos (m3). Como 1 bar é igual a 100.000 Pascal (1,00 × 105 Pa), conforme indicado na tabela de conversão, podemos empregar uma regra de três simples para converter 1.800 bar em Pascal, conforme demonstrado a seguir:
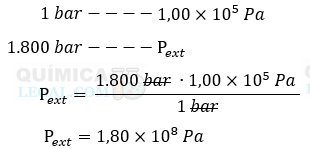
Agora, sabendo que 1 L é igual a 0,001 m3 (1 × 10−3 m3), conforme mostrado na tabela de conversão, podemos utilizar outra regra de três para converter 3,6 L em m3, como mostrado abaixo:

Ao substituir os valores na fórmula do trabalho, obtemos:

Sendo assim, a cada segundo, um pistão realiza −6,48 × 105 J de trabalho. Dessa forma, para determinar o trabalho dos quatro pistões operando ao longo de um minuto (60 segundos), realizamos o seguinte cálculo:
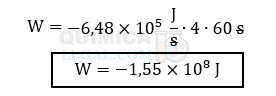
Portanto, o motor é capaz de produzir um total de −1,55 × 108 joules de trabalho em 1 minuto.
b) Quando energia é transferida para um sistema na forma de trabalho, sua energia interna aumenta e o trabalho (W), por convenção, é considerado positivo (W > 0). Por outro lado, quando a energia deixa o sistema na forma de trabalho, sua energia interna diminui e o trabalho é negativo (W < 0). No contexto de uma expansão, em que o sistema realiza trabalho sobre o ambiente, ocorre a saída de energia do sistema na forma de trabalho. Portanto, o trabalho realizado é negativo.



