Na natureza nada se cria, nada se perde…
(UERJ) “Na natureza nada se cria, nada se perde; tudo se transforma.” Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em que foi formulado, sua validade foi contestada, já que na queima de diferentes substâncias era possível observar aumento ou diminuição de massa.
Para exemplificar esse fenômeno, considere as duas balanças idênticas I e II mostradas na figura a seguir. Nos pratos dessas balanças foram colocadas massas idênticas de carvão e de esponja de aço, assim distribuídas:
- pratos A e C: carvão;
- pratos B e D: esponja de aço.
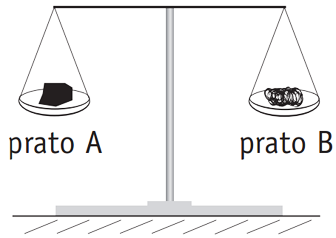 | 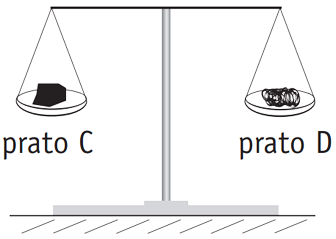 |
I | II |
A seguir, nas mesmas condições reacionais, foram queimados os materiais contidos em B e C, o que provocou desequilíbrio nos pratos das balanças. Para restabelecer o equilíbrio, serão necessários procedimentos de adição e retirada de massas, respectivamente, nos seguintes pratos:
a) A e D
b) B e C
c) C e A
d) D e B
Resolução
É conhecido que a esponja de aço consiste principalmente de átomos de ferro (Fe). Portanto, podemos descrever a reação de combustão desse material por meio da seguinte equação química balanceada:
4 Fe(s) + 3 O2(g) → 2 Fe2O3(s)
Conforme indicado na equação, o produto resultante da reação é formado pela combinação dos átomos de ferro presentes na palha de aço com o oxigênio presente no ar. Como resultado, a massa do produto é superior à massa inicial da palha de aço. Isso fará com que o prato B da balança desça, enquanto o prato A se elevará.
Na balança 2, o material que passou pelo processo de combustão foi o carvão, localizado no prato C. O carvão é composto predominantemente por átomos de carbono (C), e, portanto, a reação de combustão desse material pode ser representada por meio da seguinte equação química balanceada:
C + O2(g) → CO2(g)
Neste caso, o produto resultante é gasoso e escapa para a atmosfera, deixando apenas as cinzas no prato C. Consequentemente, após a reação, a massa do prato C diminui, causando um desequilíbrio na balança, com o prato C se movendo para baixo.
Portanto, para reequilibrar as balanças, é necessário adicionar massa ao prato A e remover massa do prato B.
Confira mais EXERCÍCIOS RESOLVIDOS sobre REAÇÕES QUÍMICAS.
Veja também: EXERCÍCIOS DE QUÍMICA GERAL E INORGÂNICA
Gostaria de ver mais RESOLUÇÕES COMENTADAS da UERJ?



