O hipoclorito de sódio tem propriedades bactericida e…
(ESPM-SP) O hipoclorito de sódio tem propriedades bactericida e alvejante, sendo utilizado para cloração de piscinas, e é vendido no mercado consumidor em solução como Água Sanitária, Cândida, Q-Boa, etc. Para fabricá-lo, reage-se gás cloro com soda cáustica:
Cℓ2(g) + 2 NaOH(aq) → NaCℓ(aq) + NaCℓO(aq) + H2O(ℓ)
A massa de soda cáustica, NaOH, necessária para obter 149 kg de hipoclorito de sódio, NaCℓO, é:
Dados: H = 1 u; O = 16 u; Na = 23 u; CL = 35,5 u
a) 40 kg
b) 80 kg
c) 120 kg
d) 160 kg
e) 200 kg
Utilize a tabela periódica para calcular as massas molares quando necessário.
Resolução
De acordo com a equação química, já balanceada, é produzido 1 mol de NaCℓO para cada 2 mols de NaOH consumidos. Assim, temos:
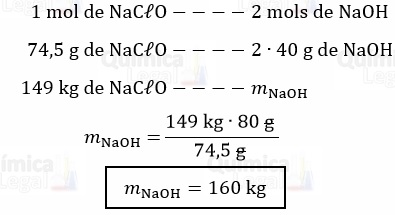
Gabarito: LETRA D
Confira mais EXERCÍCIOS RESOLVIDOS de ESTEQUIOMETRIA.
Tá afim de ver mais RESOLUÇÕES COMENTADAS da ESPM-SP?



